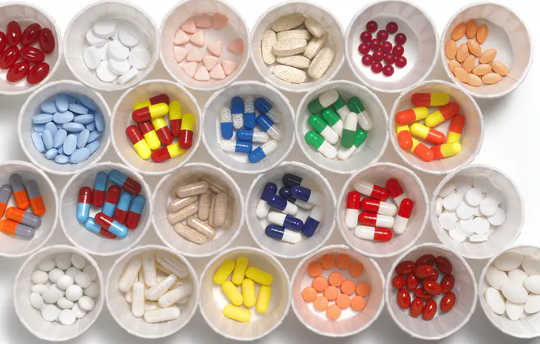
Υπάρχουν πολλά περισσότερα συστατικά σε κάθε χάπι που παίρνετε από ό, τι αναφέρεται στην ετικέτα της φιάλης. Αυτά τα άλλα συστατικά, τα οποία συνδυάζονται με το θεραπευτικό, προέρχονται συχνά από όλο τον κόσμο πριν προσγειωθούν στο φαρμακείο σας και δεν είναι πάντα καλοήθη.
Νωρίτερα φέτος, το Κογκρέσο των ΗΠΑ πέρασε το Coronavirus Aid, Relief και Economic Security Act, το οποίο απαιτεί από τους κατασκευαστές αναφέρετε πραγματικές ή πιθανές ελλείψεις φαρμάκων στο FDA. Οι κατασκευαστές καλούνται τώρα να αναφέρουν διαταραχές στην παρασκευή ενός δραστικού φαρμακευτικού συστατικού - το μέρος του φαρμάκου που παράγει το επιδιωκόμενο θεραπευτικό όφελος.
Αλλά ο νόμος CARES δεν περιλαμβάνει έκδοχα - τα «ανενεργά» συστατικά που αποτελούν το μεγαλύτερο μέρος ενός τελικού φαρμάκου. Επίσης, δεν περιλαμβάνει τα υλικά που απαιτούνται για τη συσκευασία και τη διανομή ιατρικών προϊόντων, όπως φιαλίδια και άλλα δοχεία, συσκευασίες και ετικέτες. Ενώ ο νόμος CARES βελτιώνει τη ροή πληροφοριών και μπορεί να σηματοδοτήσει πιθανές ελλείψεις φαρμάκων, προορίζεται να υποστηρίξει τις ρυθμιστικές αρχές (όπως το FDA) στις ευθύνες τους για τη δημόσια υγεία. Δεν αυξάνει τη διαφάνεια στους καταναλωτές φαρμάκων.
Ως εκπαιδευμένος φαρμακοποιός και ερευνητής που ενδιαφέρεται να αποκαλύψει κινδύνους για την ποιότητα του φαρμάκου, πιστεύω ότι οι ασθενείς και οι κλινικοί ιατροί θα ωφεληθούν από το να έχουν περισσότερες πληροφορίες σχετικά με όλα τα συστατικά στην ιατρική. Αλλά για να συμβεί αυτό απαιτούνται πρόσθετα μέτρα αύξηση της διαφάνειας για όλα τα συστατικά ενός φαρμάκου, συμπεριλαμβανομένων των εκδόχων.
Επισήμανση προϊόντος για «ανενεργά» συστατικά
Ως τα λεγόμενα «ανενεργά» συστατικά στα φάρμακα, τα έκδοχα συχνά εκλαμβάνονται ως απαλλαγμένα από πιθανές βλάβες. Αλλά τα στοιχεία δείχνουν το αντίθετο. Μεταξύ 2015 και 2019, οι επαγγελματίες υγείας, οι ασθενείς και οι κατασκευαστές υπέβαλαν σχεδόν αίτηση 2,500 αναφορές στο FDA σχετικά με μια ανεπιθύμητη ενέργεια σε ένα έκδοχο.
Ενώ τα έκδοχα αναφέρονται στη συσκευασία ή στο ένθετο συσκευασίας για φάρμακα χωρίς συνταγή και συνταγογραφούμενα φάρμακα, αυτές οι πληροφορίες μπορεί να είναι δύσκολο να βρεθούν. Επιπλέον, οι ασθενείς συχνά αλλάζουν από εμπορικό σήμα σε γενικές εκδόσεις, ή ο φαρμακοποιός αντικαθιστά έναν κατασκευαστή από έναν άλλο. Ενώ το δραστικό φαρμακευτικό συστατικό παραμένει το ίδιο, τα έκδοχα μπορεί να είναι διαφορετικά και ακόμη και φαινομενικά μικρές διαφορές μπορούν να επηρεάσουν σημαντικά την ασφάλεια των ασθενών. Για παράδειγμα, ένας ασθενής μπορεί να είναι αλλεργικός σε ένα έκδοχο στο πρόσφατα ξαναγεμισμένο φάρμακο με διαφορετικό κατασκευαστή.
Τα έκδοχα είναι κρίσιμα υλικά και εξυπηρετούν μια μεγάλη ποικιλία λειτουργιών. Χρησιμεύουν ως πληρωτικά, βοηθούν το σώμα να απορροφήσει το φάρμακο και προσθέτει γεύση ή χρώμα στα φάρμακα. Στην πραγματικότητα, ορισμένα βρίσκονται συχνά σε προϊόντα διατροφής, όπως λακτόζη, φυστικέλαιο και άμυλο. Στις Ηνωμένες Πολιτείες, τα έκδοχα εγκρίνονται από το FDA ως μέρος της διαδικασίας αναθεώρησης του τελικού φαρμάκου. Θεωρούνται από τον ρυθμιστικό οργανισμό ως γενικά αναγνωρισμένο ως ασφαλές ή «GRAS». Ωστόσο, μια πλήρης εικόνα της κλινικής τους επίδρασης παραμένει ασαφής.
Έρευνες από το MIT και το Brigham and Women's Hospital διαπίστωσαν ότι 92.8% των από του στόματος φαρμάκων περιέχουν τουλάχιστον ένα πιθανό αλλεργιογόνο, μια ανησυχία για άτομα με γνωστές ευαισθησίες και δυσανεξίες. Το πρόσφατο μου έρευνα, διερεύνηση της ασφάλειας των εκδόχων στη βιολογία, τα οποία είναι μεγάλα σύνθετα μόρια που χορηγούνται ως επί το πλείστον μέσω ένεσης, διαπίστωσαν αναφορές περιπτώσεων αντίδρασης στο σημείο της ένεσης, σοβαρή αλλεργική αντίδραση, αύξηση του επιπέδου σακχάρου στο αίμα και οξεία νεφρική ανεπάρκεια που σχετίζονται με αυτά τα «ανενεργά» συστατικά.
Παρά τις ενδείξεις ότι τα έκδοχα είναι υπεύθυνα για αντιδράσεις φαρμάκων, η ποσότητα κάθε εκδόχου που προστίθεται σε κάθε φάρμακο δεν αναφέρεται για σχεδόν το ήμισυ των βιολογικών φαρμάκων. Στην πραγματικότητα, η μελέτη μας διαπίστωσε ότι Το 44.4% των βιολογικών ετικετών δεν αναφέρει τη συγκέντρωση από τα πιο συχνά εμφανιζόμενα έκδοχα. Αυτό ισχύει για όλα τα συνταγογραφούμενα φάρμακα, όχι μόνο για τους βιολόγους.
Αυτή η έλλειψη πληροφοριών έχει σημαντικές επιπτώσεις σε ασθενείς με ασθένειες που προκαλούν διατροφικούς περιορισμούς - όπως δυσανεξία στη γλουτένη ή στη λακτόζη, τροφικές αλλεργίες ή διαβήτη - επειδή η ποσότητα αμύλου σίτου, λακτόζης, φυστικέλαιου και γλυκόζης στο φάρμακο τους μπορεί να είναι δυνητικά επιβλαβής.
Επέκταση της διαφάνειας στις πηγές φαρμάκων και στα συστατικά τους
Οι ετικέτες συσκευασίας τροφίμων πρέπει να περιέχουν το όνομα, τη διεύθυνση και τον αριθμό τηλεφώνου του κατασκευαστή μαζί με τη λίστα συστατικών. Αυτές οι πληροφορίες επιτρέπουν στους καταναλωτές να επικοινωνούν απευθείας με τους κατασκευαστές για να ρωτήσουν σχετικά με την πηγή των συστατικών του προϊόντος και να ενημερώσουν την εταιρεία για τυχόν γνωστές ή πιθανές αντιδράσεις στα συστατικά. Σε περίπτωση ανάκλησης, οι πληροφορίες σχετικά με την πηγή τροφίμων παρέχουν επίσης κρίσιμες πληροφορίες στους υπαλλήλους της δημόσιας υγείας, επιτρέποντάς τους να ειδοποιούν το κοινό σχετικά με δυνητικά μολυσμένα είδη τροφίμων με ειδικότητα.
Αυτό δεν ισχύει για τα ιατρικά προϊόντα, παρόλο που η πηγή των συστατικών του φαρμάκου είναι εξίσου σημαντική, αν όχι περισσότερο, όπως και για τα τρόφιμα.
Η FDA Νόμος για την ασφάλεια και την καινοτομία του 2012 ανέθεσαν στους κατασκευαστές ναρκωτικών να υποβάλλουν πληροφορίες σχετικά με προμηθευτές εκδόχων, συμπεριλαμβανομένων ονομάτων, διευθύνσεων και στοιχείων επικοινωνίας. Ωστόσο, επειδή αυτές οι πληροφορίες θεωρούνται «ιδιόκτητες» για τον κατασκευαστή, δεν αποκαλύπτονται δημοσίως. Ενώ το FDASIA ήταν ένα βήμα προς τη διαφάνεια της αλυσίδας εφοδιασμού, εξακολουθεί να αφήνει τους ασθενείς και τους επαγγελματίες του τομέα της υγείας χωρίς πληροφορίες που θα μπορούσαν να είναι κρίσιμες.
Πιθανές πολιτικές διαφάνειας για τη βελτίωση της ασφάλειας των ασθενών
Σε ένα ερευνητικό έγγραφο που μελετά τους κινδύνους που σχετίζονται με τα έκδοχα, ο συν-συγγραφέας μου και εγώ Κάντε τρεις κύριες συστάσεις για τη βελτίωση της ασφάλειας των ασθενών.
Πρώτον, οι απαιτήσεις αναφοράς παρόμοιες με εκείνες για τα τρόφιμα και τα δραστικά φαρμακευτικά συστατικά πρέπει να επεκτείνονται στα έκδοχα. Δεύτερον, οι γιατροί και οι ασθενείς θα πρέπει να έχουν εύκολη πρόσβαση σε αυτές τις πληροφορίες, συμπεριλαμβανομένων των ποσοτήτων και των πιθανών ανεπιθύμητων ενεργειών. Στο κοινό θα πρέπει επίσης να παρέχονται πληροφορίες σχετικά με τον τρόπο με τον οποίο θα αναφερθούν πλήρως και με ακρίβεια οι ανεπιθύμητες ενέργειες που σχετίζονται με έκδοχα. Τρίτον, οι ρυθμιστικοί οργανισμοί πρέπει να παρέχουν καθοδήγηση για την αναφορά εκδόχων, διευκολύνοντας μεγαλύτερη διαφάνεια σχετικά με τη χρήση και την πηγή εφοδιασμού των εκδόχων.![]()
Σχετικά με το Συγγραφέας
Yelena Ionova, μεταδιδακτορικός συνεργάτης στην ποιότητα των ιατρικών προϊόντων, Πανεπιστήμιο της Καλιφόρνια, Σαν Φρανσίσκο
Αυτό το άρθρο αναδημοσιεύθηκε από το Η Συνομιλία υπό την άδεια Creative Commons. Διαβάστε το αρχικό άρθρο.
βιβλία_συμπληρώματα